Os lipossomas foram descobertos pela primeira vez pelo hematologista britânico Alec D. Bangham em 1965. Ao estudar o comportamento de dispersão dos fosfolipídios na água, ele observou que as moléculas de fosfolipídeos formaram espontaneamente estruturas de vesículas multicamadas semelhantes às das membranas biológicas. Naquela época, a pesquisa se concentrou principalmente em físico-química básica e simulação de membrana biológica.
Os pesquisadores começaram a perceber que os lipossomas poderiam encapsular substâncias solúveis em água e solúveis em lipídios, fornecendo um portador potencial para a administração de drogas. Por exemplo, em laboratório, moléculas de modelo de droga simples, como corantes fluorescentes, foram encapsuladas em lipossomas para observar suas características de encapsulamento e liberação.
Com uma maior compreensão da estrutura e propriedades dos lipossomas, suas aplicações na área médica começaram a ser exploradas. Este período se concentrou principalmente na entrega de medicamentos antitumorais.
Por exemplo, alguns medicamentos quimioterapêuticos, como a doxorrubicina, foram encapsulados em lipossomas, tentando alterar a farmacocinética e a distribuição tecidual dos medicamentos por meio do encapsulamento de lipossomas, e reduzir a toxicidade das drogas para os tecidos normais. No entanto, os primeiros lipossomas tinham problemas como baixa estabilidade e serem facilmente eliminados pelo sistema mononuclear-fagócito (MPS). Eles tiveram um curto tempo de circulação no corpo e foram liberados pelo sistema imunológico antes que pudessem exercer totalmente sua eficácia, o que limitou muito suas aplicações clínicas.
Para superar o problema do curto tempo de circulação dos lipossomas tradicionais no corpo, os cientistas introduziram a tecnologia dos lipossomas modificados por polietilenoglicol (PEG). PEG é um polímero hidrofílico. Quando está ligado à superfície dos lipossomas, pode formar uma película hidratada ao redor dos lipossomas.
Este filme hidratado pode reduzir a interação entre os lipossomas e as proteínas plasmáticas, reduzindo assim o reconhecimento e a absorção de lipossomas pelo sistema mononuclear-fagócito. Por exemplo, o Doxil, o primeiro medicamento lipossômico de longa circulação comercializado no mundo, é um lipossoma modificado por PEG que encapsula doxorrubicina. O surgimento do Doxil estendeu muito o tempo de circulação dos lipossomas no sangue, permitindo que os medicamentos tenham mais oportunidades de atingir os tecidos tumorais e melhorando o efeito terapêutico dos medicamentos.
Os pesquisadores conduziram estudos aprofundados sobre lipossomas modificados por PEG, incluindo a otimização do peso molecular do PEG, o método de conexão e a composição dos lipossomas.
Ao mesmo tempo, o escopo de aplicação de lipossomas de longa circulação se expandiu de drogas antitumorais para outros campos, como a administração de antiinflamatórios e antibióticos. Por exemplo, no tratamento de algumas doenças inflamatórias crônicas, os lipossomas de longa circulação que encapsulam os antiinflamatórios podem fazer com que os medicamentos se acumulem melhor nos locais inflamatórios, aumentar a concentração local de drogas, e reduzir os efeitos colaterais sistêmicos.
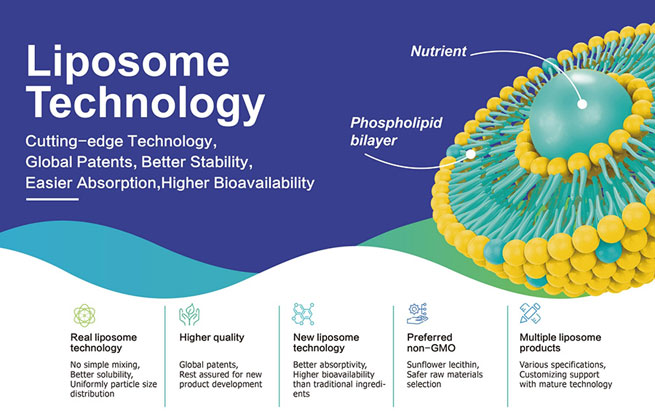
Para melhorar ainda mais o efeito terapêutico dos lipossomas e permitir que eles distribuam drogas com mais precisão às células doentes, surgiu a tecnologia dos lipossomas direcionados. Entre eles, a conjugação de anticorpos à superfície dos lipossomas é uma estratégia importante.
Por exemplo, ao conectar anticorpos contra antígenos específicos na superfície das células tumorais à superfície dos lipossomas, os lipossomas podem reconhecer e se ligar com precisão às células tumorais como "mísseis". Este lipossoma direcionado pode aumentar a absorção de drogas nas células tumorais e reduzir sua distribuição nos tecidos normais. Foi aplicado na pesquisa de tratamento de vários tipos de câncer, como câncer de mama e câncer de pulmão.
Além dos anticorpos, outros ligantes também podem ser usados para atingir o direcionamento de lipossomas. Por exemplo, alguns ligantes de pequenas moléculas, como ácido fólico e transferrina, podem ser utilizados. O receptor de ácido fólico é superexpresso na superfície de muitas células tumorais, enquanto é expresso em um nível relativamente baixo na superfície das células normais.
Portanto, ao conectar o ácido fólico à superfície dos lipossomas para administrar drogas, os lipossomas podem se ligar preferencialmente às células tumorais. Este sistema de direcionamento ligante-lipossoma tem vantagens como custo relativamente baixo e preparação fácil, e também tem sido amplamente aplicado na pesquisa de tratamento de tumores e algumas outras doenças (como doenças cerebrais, usando transferrina para direcionar os receptores da barreira hematoencefálica).
Os lipossomas inteligentes podem alterar sua estrutura e propriedades de acordo com as mudanças no ambiente circundante, como pH, temperatura e concentração de enzimas. No microambiente tumoral, o pH geralmente é menor do que nos tecidos normais. Os lipossomas responsivos ao pH podem tirar proveito dessa característica.
Por exemplo, um lipossoma sensível ao pH pode ser projetado para permanecer estável em condições normais de pH fisiológico. Quando atinge o microambiente ácido do tumor, a estrutura do lipossoma muda, como um aumento na permeabilidade da membrana, liberando rapidamente a droga. Este tipo de lipossoma responsivo ao ambiente pode melhorar a eficiência da liberação do medicamento no local da lesão e aumentar ainda mais o efeito terapêutico.
Os lipossomas multifuncionais combinam várias funções, como longa circulação, direcionamento e capacidade de resposta ao meio ambiente. Por exemplo, um lipossoma pode ter simultaneamente modificação de PEG para estender o tempo de circulação, anticorpos para células tumorais alvo e um mecanismo de liberação de medicamento sensível ao pH.
O conceito de design deste lipossoma multifuncional é maximizar a precisão e eficácia da entrega do medicamento. Possui grande potencial de aplicação em cenários complexos de tratamento de doenças, como terapia tumoral combinada ou terapia multialvo.
Os lipossomas co-carregados de Campo Natural pertencem à tecnologia inovadora de lipossomas inteligentes, usando ginsenosídeos em vez de colesterol como um novo tipo de portador, que pode atingir maior biodisponibilidade.